技術コラム ポンプの基礎知識クラス
ポンプの基礎知識クラス
【A-7c】
ステンレス鋼の腐食形態について
ポンプの基礎知識のクラスを受け持つ、ティーチャー モーノベです。
今回はステンレス鋼の腐食のさまざまな形態について、掘り下げて説明したいと思います。
金属の腐食ついて
ステンレス鋼の腐食について話す前に、まずは金属の腐食のしくみについて鉄を例に説明します。腐食とは金属が使用環境において、電気化学的な反応によって侵食される現象のことをいい、酸化反応(アノード反応)と同時に還元反応(カソード反応)を伴います。
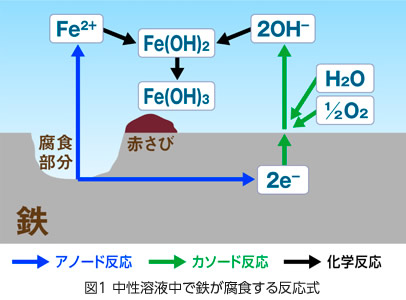
腐食が進行する際、鉄(Fe)は鉄イオン(Fe2+)となって溶液中に移行するとともに電子(2e-)を放出します(1)。
これに対して、pHが低く、水素イオン(2H+)が十分存在する場合には、水素イオン(2H+)は鉄(Fe)がイオン化した時に放出した電子(2e-)を受け取り、水素ガス(H2)となります(2)。
また、pHが中性近辺の場合には、反応の主体は溶液中の酸素(1/2O2)となって、電子(2e-)を受けとり、水酸化物イオン(2OH-)となります(3)。
これが金属の腐食のしくみで、電池作用や腐食電池と呼ばれます。
- アノード反応
- (1) Fe → Fe2+ + 2e-
- カソード反応
- (2) 2H+ + 2e- → H2
- (3) 1/2O2 + H2O + 2e- → 2OH-
中性溶液中で鉄が腐食する場合を考えると、腐食の全反応は(1)と(3)の式の和として得られます。この場合、イオン化した鉄(Fe2+)と水酸化物イオン(2OH-)が結合し、水酸化第一鉄(Fe(OH)2)が析出します。また析出した水酸化第一鉄(Fe(OH)2)は溶液中の酸素(1/2O2)によって酸化され、水酸化第二鉄(Fe(OH)3)となり、赤さびのもととなります。
ステンレス鋼の腐食について
ステンレス鋼が酸化皮膜(不動態皮膜)の形成により優れた耐食性を示すことは前回の講義ですでにお話ししていますが、ステンレス鋼であっても適さない環境や用途では腐食が進行しますので、注意が必要です。
ステンレス鋼の腐食形態は、全面腐食と局部腐食に分けられます。全面腐食は塩酸や希硫酸にさらされるなど、不動態皮膜ができにくい環境で発生します。メカニズムとしては、最初に説明した、アノード反応・カソード反応と同じです。一方、局部腐食とは、環境条件によって局所的に不動態皮膜が破壊されることで発生する腐食です。特に塩化物イオンの存在により、局部腐食は進行します。
ステンレス鋼の局部腐食の形態について
ステンレス鋼の局部腐食には以下の種類があります。
1.孔食/すきま腐食
孔食は、表面が局部的に点、または孔状に深く侵食される現象です。溶液中の塩化物イオンの影響で、ステンレス鋼の表面に付着した異物などを起点として、局所的に不動態皮膜が破壊され、その部分がアノード反応、他の部分がカソード反応となって局部電池をつくり、その位置が固定されて継続的に進行する場合に発生します。
すきま腐食は、フランジの接合部、パッキンの合わせ目、ガスケットのすきまなど、液が停滞しているところで腐食が孔食状に進行する現象です。すきまの内部では、酸素の供給が不十分となり、外部との間で酸素濃度に差が生じます。
すきま内部の酸素濃度の低い方がアノード反応、高い方がカソード反応となり、アノード部から溶ける、いわゆる酸素濃淡電池に起因して、塩化物イオンの存在下で不動態皮膜が破壊されます。
孔食やすきま腐食を完全に防ぐことはできませんが、さらされる環境条件を考慮して適正な材質選定を行うことで、防止対策を行います。ステンレス鋼の種類と特徴については前回の講義をご覧ください。

2.粒界腐食
前号でも紹介している通りですが、ステンレス鋼を約500~800℃に加熱すると、その近辺でクロム炭化物(Cr23C6)が析出し、クロム(Cr)が欠乏状態となります。クロム(Cr)が少ないと、耐食性が低下するため、そこから腐食を生じる現象が粒界腐食です。また、このクロム(Cr)欠乏状態のことを鋭敏化とも言います。
溶接部付近などは熱影響で特にこの鋭敏化を起こしてしまうため、溶接を実施する場合には、SUS304LやSUS316Lなどの低炭素材を用いることで、鋭敏化を防止します。
3.応力腐食割れ
鋭敏化や孔食の腐食条件下において、溶接による残留応力などの力が働いていた場合に生じます。この場合、かかる応力が材料降伏点以下であっても、腐食環境下で脆化を起こしてしまうため、割れに至ります。また、この割れを起点とし、不動態皮膜が破壊され、腐食を進行させてしまいます。
応力除去焼なましなどで残留応力を軽減したり、使用環境から溶存酸素や塩化物イオンを除去することが防止対策となります。
このように、ステンレス鋼の腐食にはさまざまな形態があります。ステンレス鋼はその特性から、高い耐食性を求められることが多いですが、前号で紹介したステンレス鋼の種類や特徴と共に、さらされる環境条件、腐食形態を想定することで、より適正な材質選定ができます。
そろそろ時間ですね!最後にまとめをしておきましょう!!
本稿のまとめ

- 高耐食のステンレス鋼でも適さない環境・用途では腐食が進行する。
- ステンレス鋼の腐食形態は全面腐食と局部腐食に分けられ、局部腐食にもさまざまな形態がある。
- ステンレス鋼の材質選定を行う場合には、ステンレス鋼の特徴だけでなく、さらされる環境条件と想定される腐食形態を考慮する必要がある。
次回はチタンやハステロイ®などの非鉄金属について、説明する予定です。
-
 ポンプの
ポンプの
基礎知識クラス
移送に関する基本情報を
わかりやすくコンパクトに
解説していきます。- 【A-1a】ポンプの種類
- 【A-1b】ポンプの種類(容積式ポンプ)
- 【A-2】ポンプの原理
- 【A-3a】軸封装置
- 【A-3b】軸封装置(メカニカルシール)
- 【A-3c】軸封装置(グランドパッキン)
- 【A-4a】NPSH(Ⅰ)
- 【A-4b】NPSH(Ⅱ)
- 【A-5】ウォーターハンマー
- 【A-6a】ポンプ選定時に確認すべき事項(1)
- 【A-6b】ポンプ選定時に確認すべき事項(2)
- 【A-6c】ポンプ選定時に確認すべき事項(3)
- 【A-7a】ポンプに使用される金属材料について
- 【A-7b】ステンレス鋼について
- 【A-7c】ステンレス鋼の腐食形態について
- 【A-7d】ポンプに使用される非鉄金属について
- 【A-8a】ポンプに使用されるゴム材料について
- 【A-8b】ゴム材料の物理的な特性
- 【A-8c】ゴム材料の化学的な特性
- 【A-9a】金属材料への表面処理
-
 ポンプの
ポンプの
周辺知識クラス
規格や周辺機器情報などを
解説していきます。- 【B-1a】ポンプの洗浄1
- 【B-1b】ポンプの洗浄2(自動洗浄における洗浄効果の因子)
- 【B-1c】ポンプの洗浄3(SIPとASEPTIC)
- 【B-2a】駆動機(駆動機の概要)
- 【B-2b】駆動機(三相交流かご形誘導モーター)
- 【B-2c】駆動機(保護方式と耐熱クラス)
- 【B-2d】駆動機(モーター技術の動向)
- 【B-2e】駆動機(変速装置・減速装置)
- 【B-2f】駆動機(番外編:周波数)
- 【B-3a】インバーターの基礎知識(Ⅰ)
- 【B-3b】インバーターの基礎知識(Ⅱ)
- 【B-3c】インバーターの基礎知識(Ⅲ)
- 【B-3d】インバーターの基礎知識(Ⅳ)
- 【B-3e】インバーターの基礎知識(Ⅴ)
- 【B-3f】インバーターの基礎知識(Ⅵ)
- 【B-4】防爆
- 【B-5】管材と計測器
- 【B-6】トップランナーモーター
- 【B-7】マグネットカップリング
-
 移送物の
移送物の
基礎知識クラス
液の特長や性状および
主な用途などを
解説していきます。 -
 IoT・AIで変わる
IoT・AIで変わる
「送る&運ぶ」
移送・搬送の現場がIoT化、
AI(人工知能)活用で
どのように変わるのか。
伊藤元昭氏が解説します。- 第1回:産業機器のIoT化で何が変わるか
- 第2回:IoTは、日本のものづくり企業こそ活用すべき
- 第3回:AI活用の本質は、匠の技やベテランの知恵の機械化
- 第4回:AI活用を円滑・効果的に進めるための鍵は現場力にあり
- 第5回:AIの「ブラックボックス問題」との付き合い方
- 第6回:5Gで加速する工場・プラントでのIoT活用
- 第7回:ものづくりのDXで、現場の仕事はどう変わるのか?①
- 第8回:ものづくりのDXで、現場の仕事はどう変わるのか?②
- 第9回:協働ロボットで作る、人と機械が助け合う現場
- 第10回:コロナ禍で加速した、ものづくりでのAI/IoT活用
- 第11回:IoT/AIを駆使して対応する脱炭素時代のものづくり
- 第12回:製造業での脱炭素化、最初に始めたいこととは
- 第13回:サプライチェーンの管理は見える化から自律化へ
- 第14回:パブリックな仮想世界、メタバースは製造業に何をもたらすのか
- 第15回:メタバース上のバーチャルファクトリーで、多方面の専門家が密に協業
- 第16回:リチウムイオン二次電池から全固体電池へ、実現の鍵を握る技術「MI」
- 第17回:電極・電解質・イオン種、全方位で進化し続ける二次電池
- 第18回:スマホや自動運転車の技術転用で、産業機器や働くクルマの自律化を実現
- 第19回:再エネ主力電源化時代が到来、大口需要家である工場に求められる備えとは
- 第20回:メンテナンス業務を再定義する、IoT遠隔監視システム
- 第21回:生成AI活用で加速する、製造業での自動設計と新素材開発
-
 現場の声で、
現場の声で、
ひとくふう
モーノポンプの使い方は現場によりさまざま。
ひとくふうを加えると、
実はおもしろい発見が!